Dalam landskap bahan maju yang sentiasa berubah, cecair ionik (ILS) telah muncul sebagai kelas bahan revolusioner yang menentang pengkategorian konvensional cecair, garam, dan pelarut. Tetapi apa sebenarnya yang menjadikan cecair ionik begitu unik-dan mengapa mereka semakin dianggap sebagai asas dalam pembangunan teknologi mampan, kimia hijau, dan sistem elektrokimia generasi akan datang?
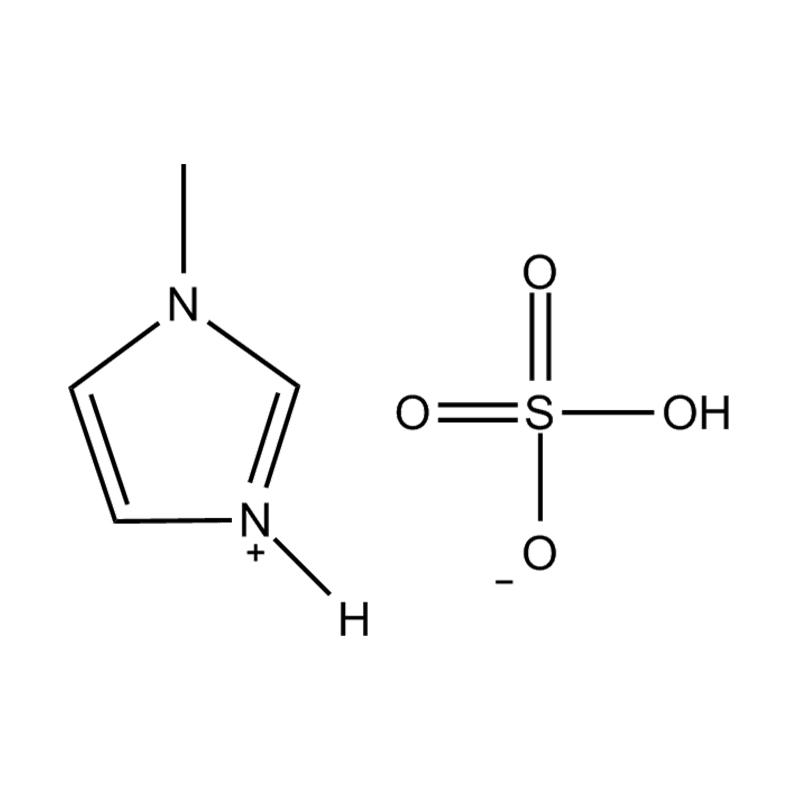
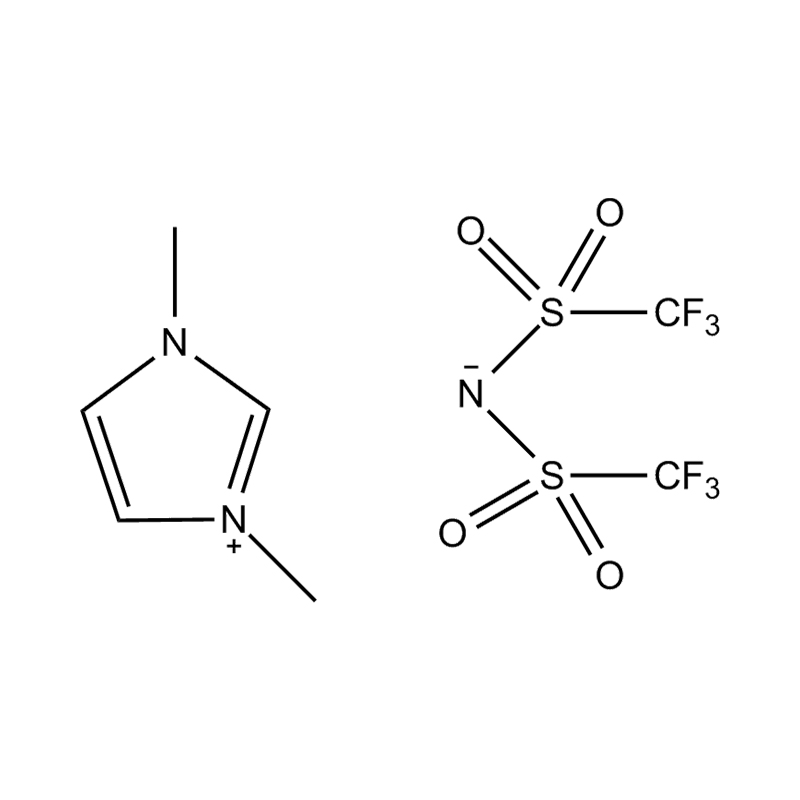
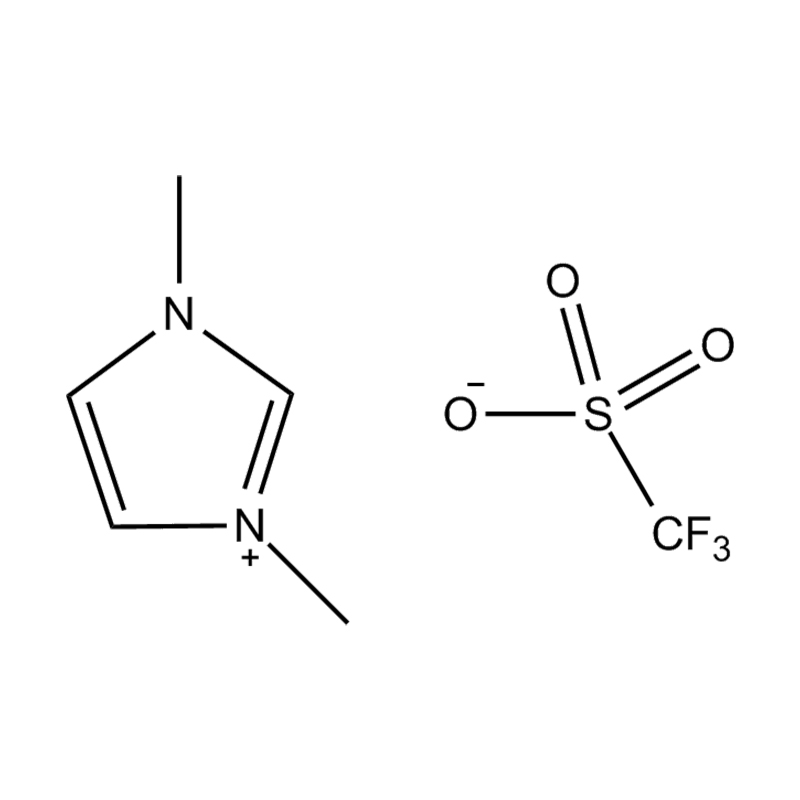
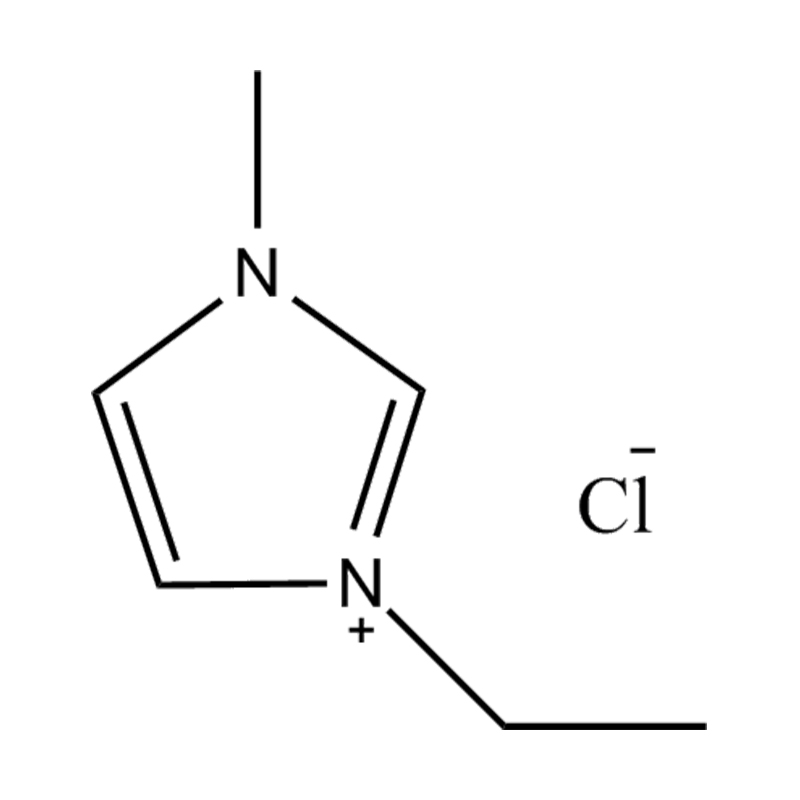
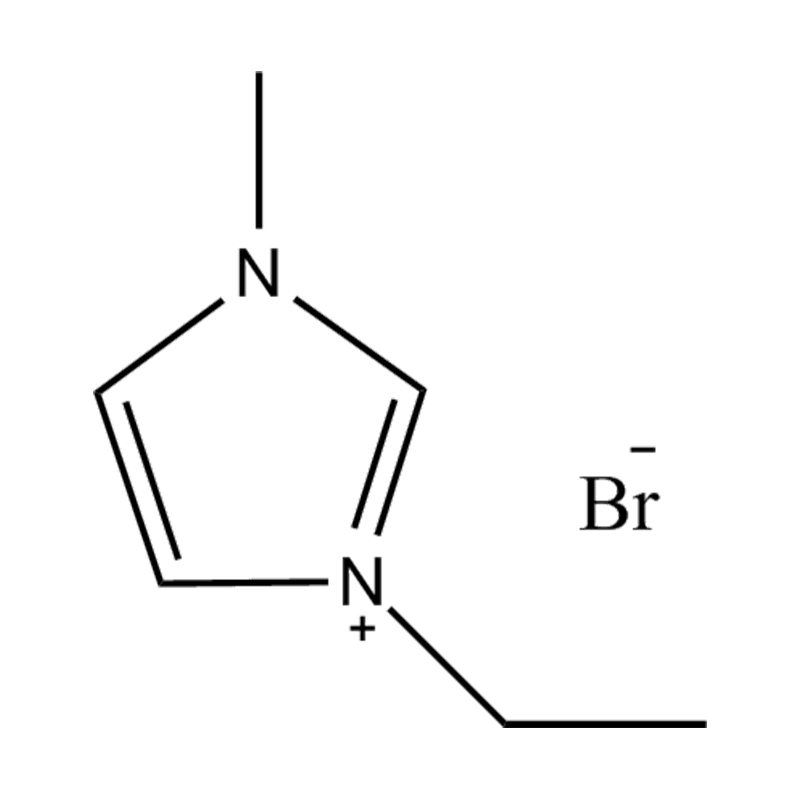
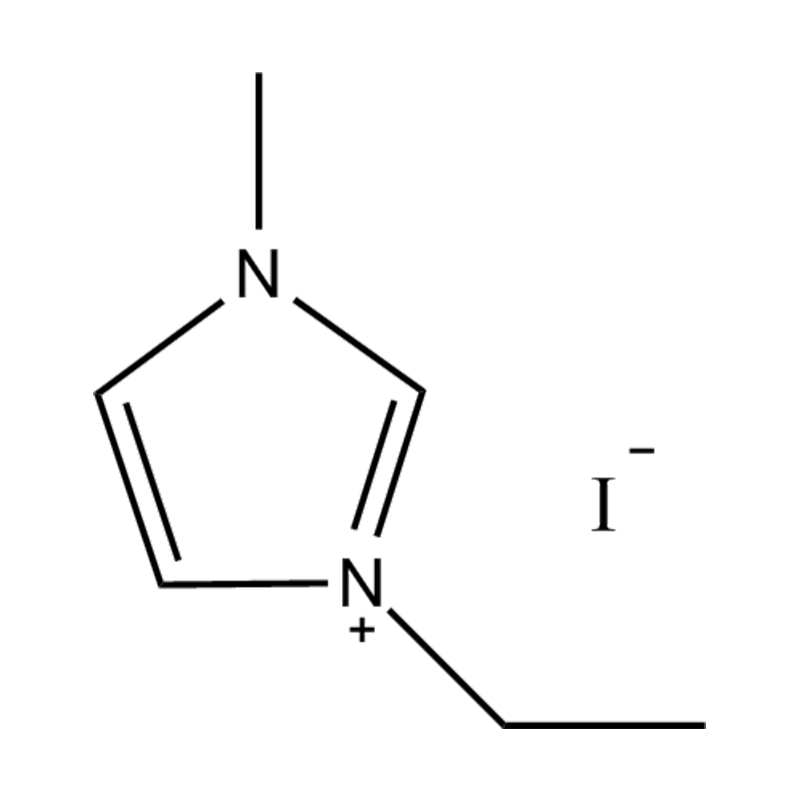
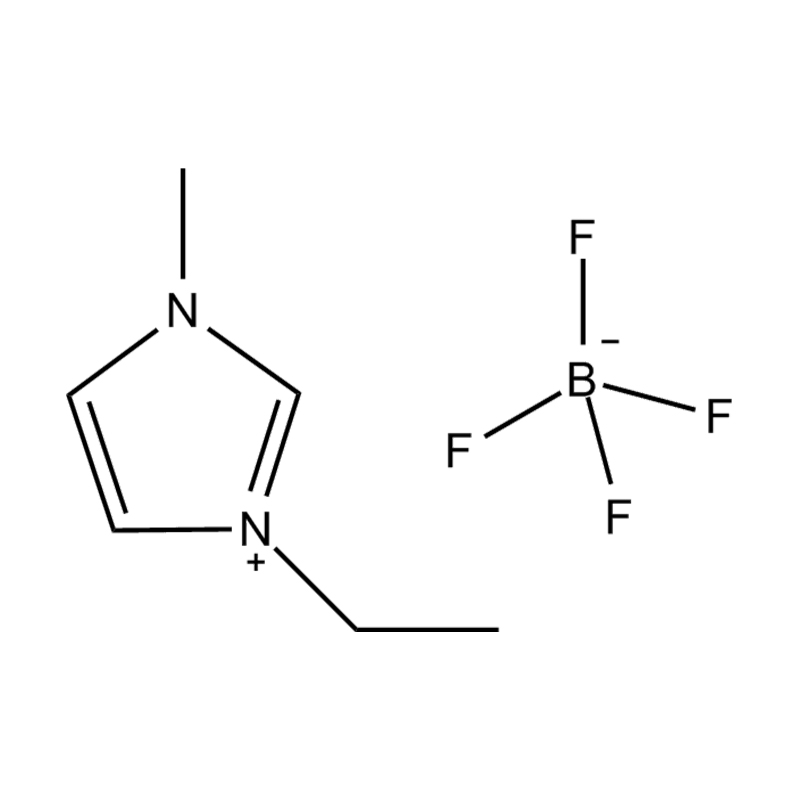
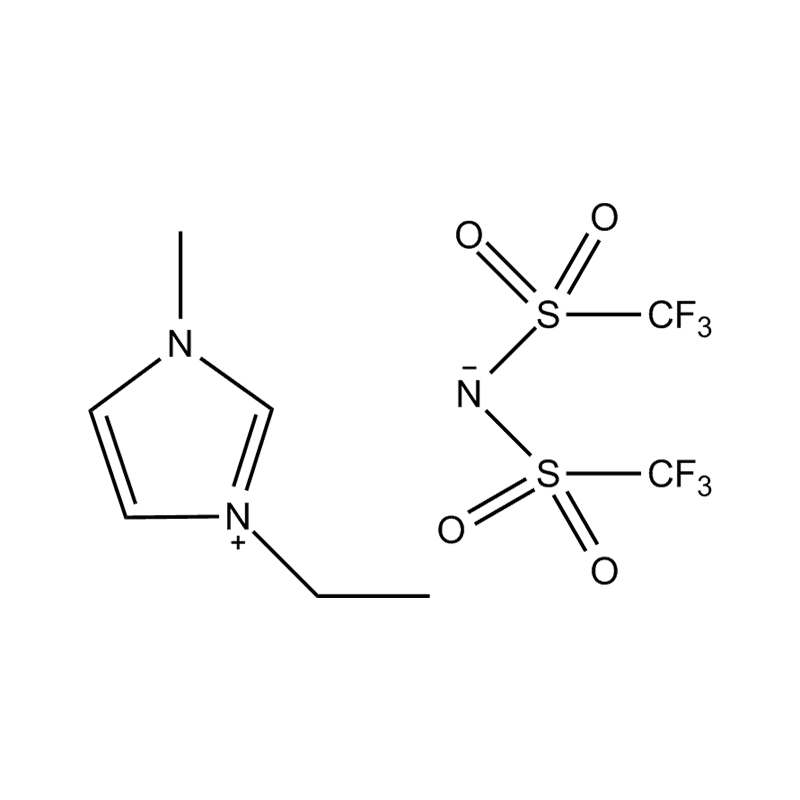
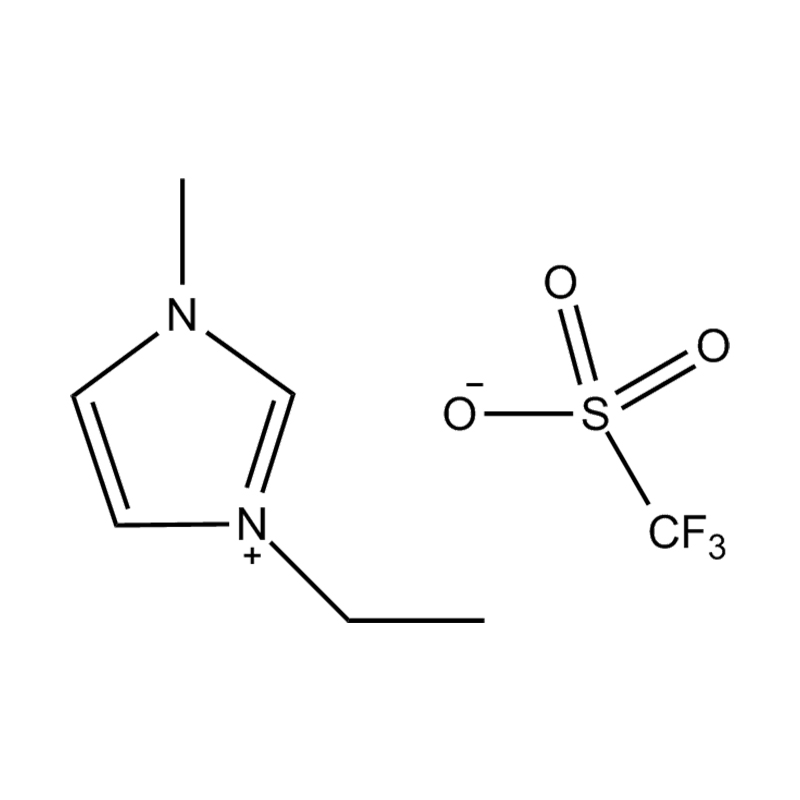
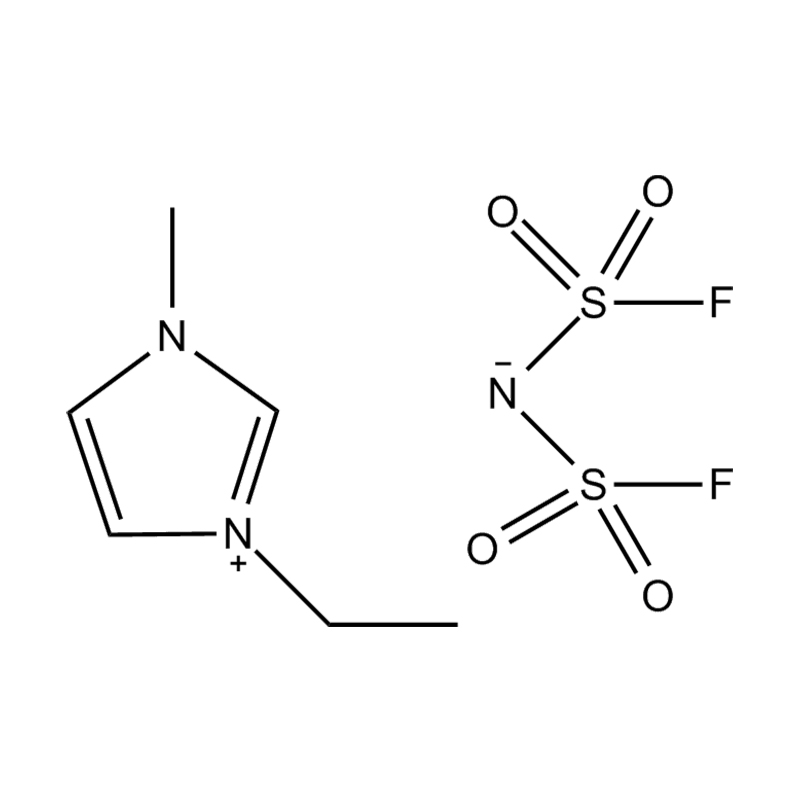
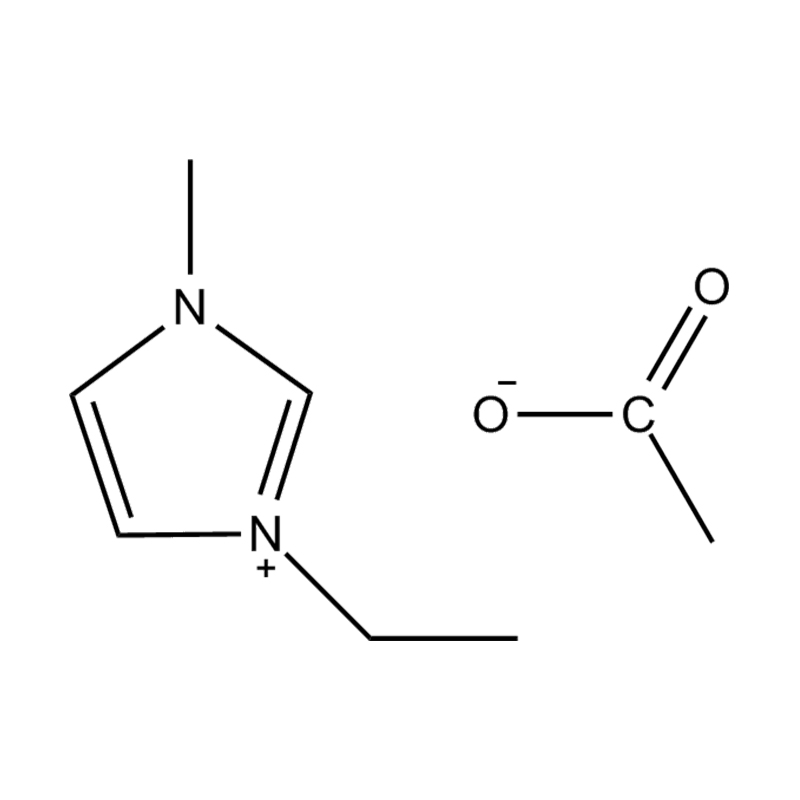
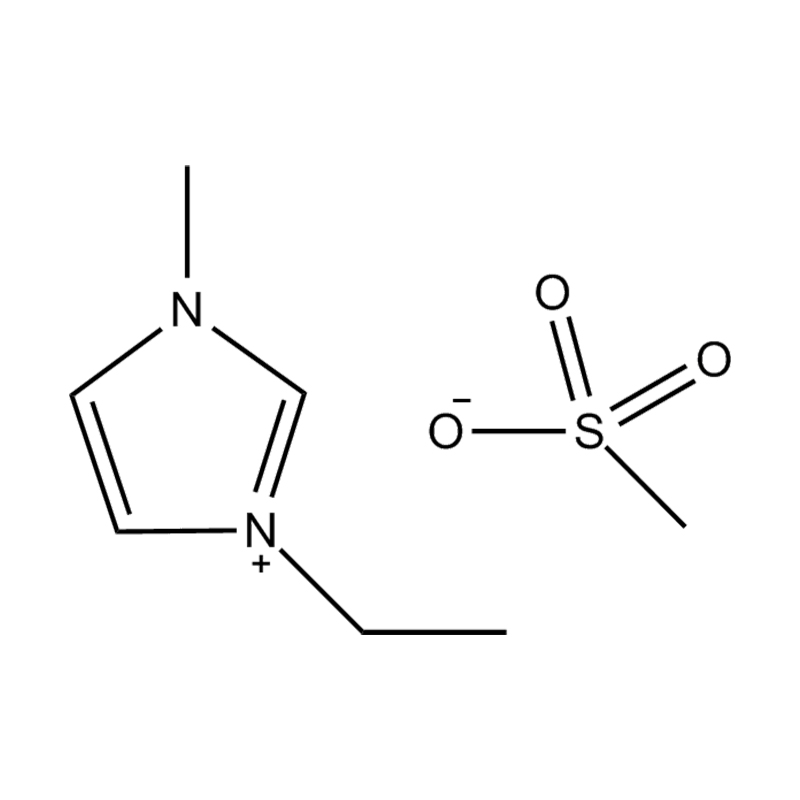
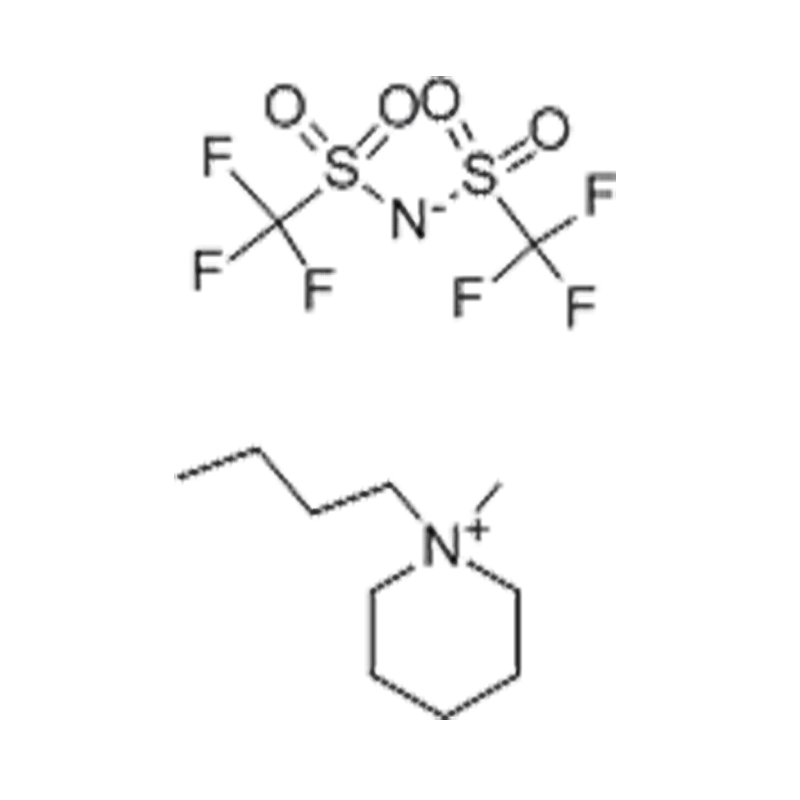
Pada tahap yang paling asas, cecair ionik adalah garam terdiri sepenuhnya daripada ion Itu kekal dalam keadaan cecair di bawah 100 ° C, selalunya walaupun pada suhu bilik. Tidak seperti garam tradisional seperti natrium klorida, yang memerlukan suhu tinggi untuk mencairkan, cecair ionik biasanya dibuat dari kation organik yang besar dan tidak simetris (seperti imidazolium, pyridinium, ammonium) yang dipasangkan dengan anion bukan organik atau organik (seperti bis (trifluoromethylsulfonyl) imide, pf₆⁻, bf₄⁻, atau halida). Bentuk yang tidak teratur dan koordinasi yang lemah antara ion menghalang penghabluran dan mengakibatkan ciri -ciri mereka yang rendah.
Ciri -ciri fizikokimia cecair ionik adalah sama seperti struktur molekul yang boleh ditukar. Salah satu ciri yang paling mendefinisikan adalah Tekanan wap yang boleh diabaikan , yang menjadikan mereka tidak berubah-ubah dan dengan itu menarik sebagai alternatif alam sekitar kepada pelarut organik tradisional. Ciri ini sahaja telah meletakkannya di barisan hadapan Dalamisiatif Kimia Hijau , di mana penghapusan sebatian organik yang tidak menentu (VOC) adalah keutamaan.
Di luar pameran cecair ionik yang tidak berubah-ubah Kestabilan terma dan elektrokimia yang luar biasa . Ramai IL boleh beroperasi pada suhu melebihi 200 ° C tanpa penguraian, dan tingkap elektrokimia yang luas (sehingga 6V dalam sesetengah sistem) menjadikannya elektrolit yang ideal dalam aplikasi seperti bateri lithium-ion, supercapacitors, dan penyaduran logam . Sifat ionik intrinsik mereka juga memberikan kekonduksian ionik yang tinggi, terutamanya dalam sistem di mana pelarut konvensional akan menguap atau merendahkan keadaan yang keras.
Satu lagi kelebihan kritikal cecair ionik terletak pada mereka keterujaan kimia . Dengan mengubah suai kation atau anion, saintis boleh menyempurnakan sifat seperti kelikatan, polariti, hidrofilik, atau keupayaan koordinasi. Ini telah membolehkan penciptaan cecair ionik khusus tugas (TSIL) Direka untuk peranan yang sangat selektif-misalnya, dalam penangkapan CO₂, pemprosesan biomas, atau pemangkinan logam peralihan. Modulariti ILS menjadikan mereka semacam "pelarut pereka" untuk persekitaran kimia yang kompleks.
Dalam bidang pemisahan dan pengekstrakan , Cecair ionik menawarkan beberapa kelebihan terhadap pelarut tradisional. Keupayaan mereka untuk melarutkan pelbagai sebatian organik dan bukan organik yang luas, ditambah pula dengan kebolehan mereka dengan air atau hidrokarbon (bergantung kepada komposisi), membolehkan sistem pengekstrakan cecair cecair yang sangat efisien. IL telah digunakan untuk Pemulihan Elemen Rangka Bumi, Penyingkiran Sebat .
In pemangkinan , kedua-duanya sebagai pelarut dan pemangkin bersama, ILS meningkatkan selektiviti dan hasil tindak balas sambil memudahkan pemisahan produk. Banyak kompleks logam peralihan mempamerkan kestabilan dan aktiviti yang lebih baik dalam media IL. Terutama, cecair ionik telah digunakan hidrogenasi asimetrik, alkilasi, dan tindak balas silang gandingan , sering di bawah keadaan yang lebih ringan daripada sistem konvensional.
Salah satu aplikasi cecair ionik yang paling canggih adalah di alam Peranti elektrokimia dan penyimpanan tenaga . Elektrolit berasaskan IL sedang dimasukkan ke dalam Bateri logam lithium, bateri natrium-ion, sel solar yang sensitif (DSSC), dan juga elektrolit keadaan pepejal . Ketidaksuburan elektrokimia mereka, ketidakmampuan, dan toleransi terma menawarkan kelebihan kritikal untuk meningkatkan keselamatan dan prestasi sistem tenaga.
Walaupun janji mereka, cecair ionik tidak tanpa cabaran. Banyak IL masih mahal untuk mensintesis secara berskala, dan ada yang menderita kelikatan tinggi , yang menghadkan kadar pemindahan massa. Di samping itu, sementara IL sering dipromosikan sebagai "pelarut hijau," mereka Biodegradability dan ketoksikan Berbeza secara meluas bergantung kepada struktur, dan kesan alam sekitar jangka panjang kekal sebagai bidang penyelidikan aktif. Menangani kebimbangan ini melalui laluan sintesis yang lebih mampan dan analisis kitaran hayat yang komprehensif akan menjadi penting untuk penggunaan yang lebih luas.
Masa depan cecair ionik semakin interdisipliner. Dalam Sains Bahan , ILS digunakan sebagai pelarut dan templat dalam sintesis nanomaterials, rangka logam-organik (MOFs), dan polimer konduktif. Dalam Bioteknologi , mereka membolehkan penstabilan enzim, pengekstrakan protein, dan juga manipulasi DNA di bawah keadaan bukan tradisional. Peranan berpotensi mereka dalam Penangkapan dan Penggunaan Karbon (CCU) Teknologi juga mendapat momentum, terutamanya memandangkan pertalian mereka untuk CO₂ dan rintangan terma yang tinggi.



 中文简体
中文简体