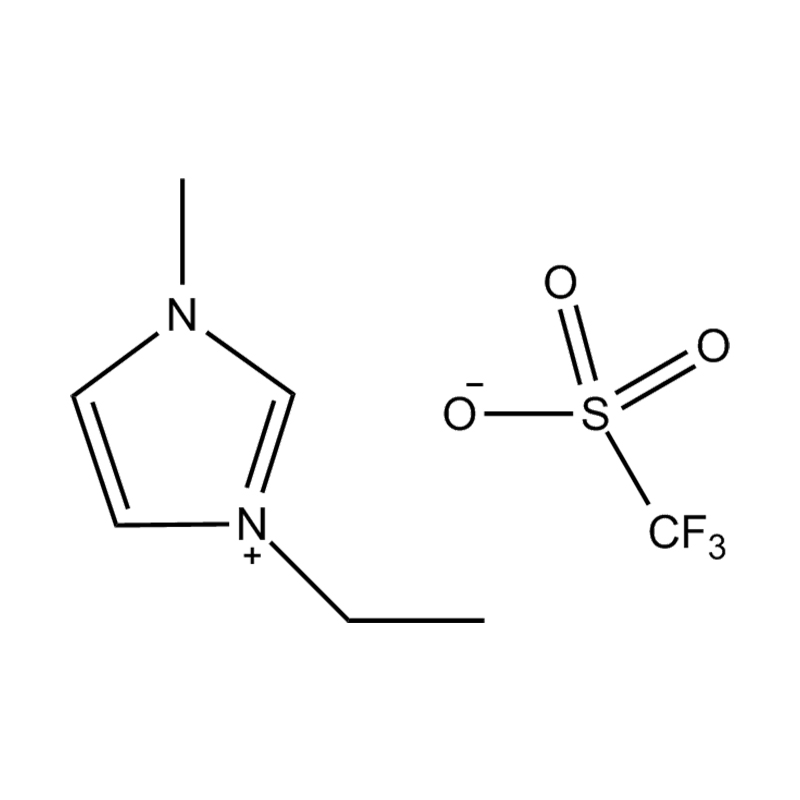
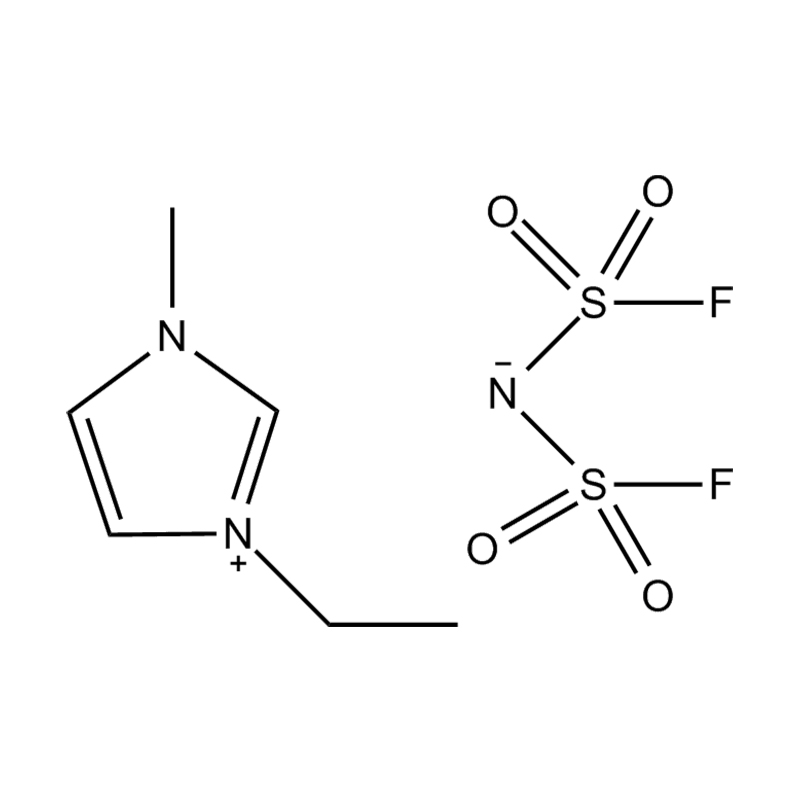
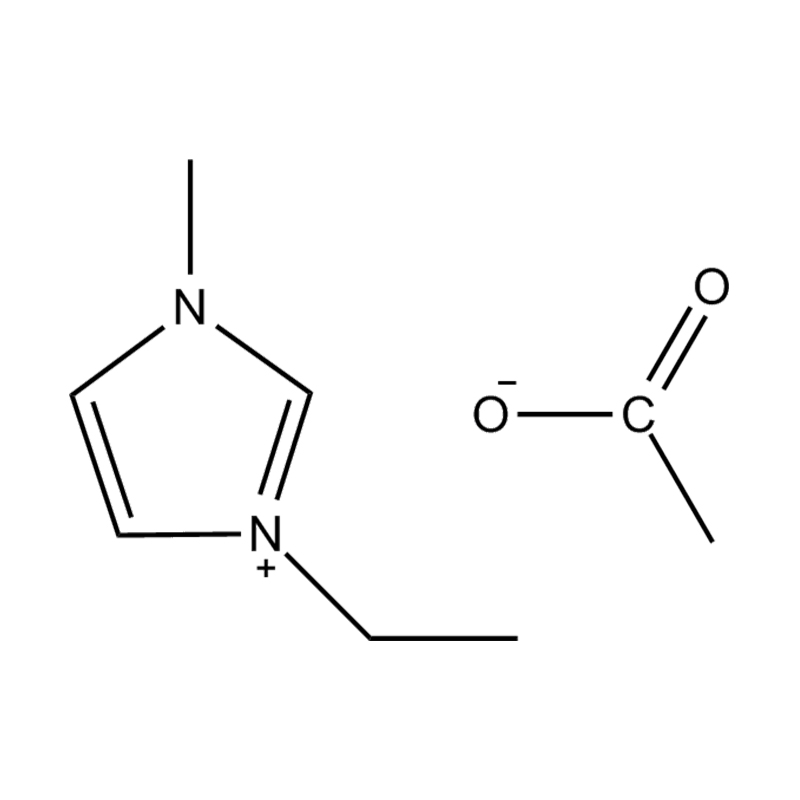
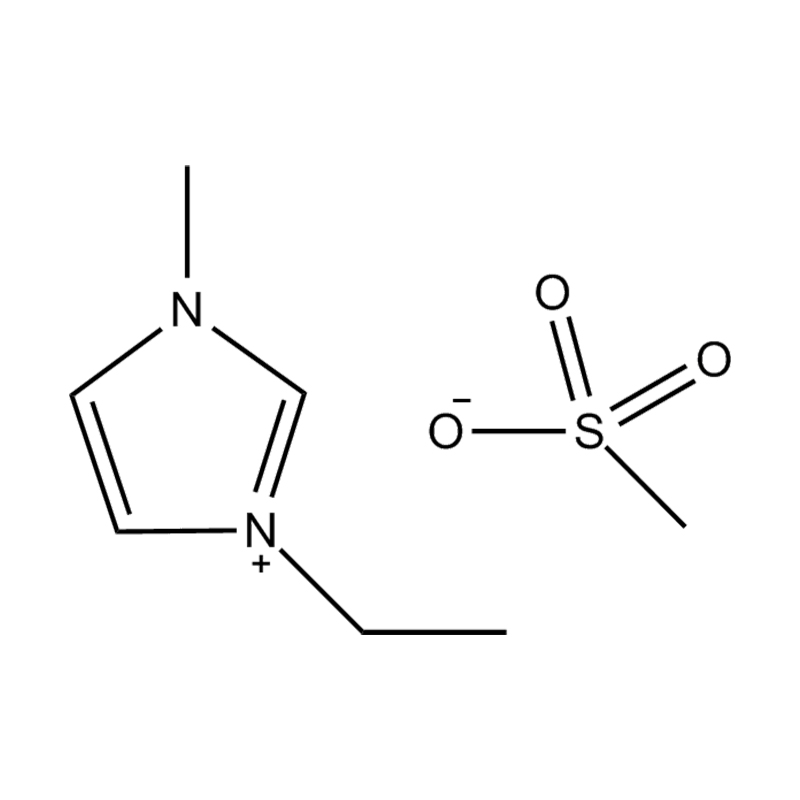
Cecair ionik pyridine (PILs), di kalangan generasi cecair ionik yang dikaji, telah menarik perhatian untuk kesederhanaan struktur dan sifat -sifat yang boleh disesuaikan. Terdiri daripada kation pyridinium dan pelbagai anion, sebatian ini menawarkan platform serba boleh untuk meneroka kimia asas cecair ionik. Walau bagaimanapun, aplikasi praktikal PIL telah dikekang oleh batasan fizikokimia tertentu -terutamanya titik lebur yang agak tinggi. Artikel ini mengkaji hubungan struktur utama yang menentukan tingkah laku PIL dan menilai potensi mereka merentasi pelbagai aplikasi kimia dan perindustrian.
Ciri -ciri struktur
Ciri penentuan cecair ionik piridin terletak pada kerangka kationik mereka. Kation biasanya merupakan ion n-alkylpyridinium, di mana panjang rantai alkil boleh berubah (mis., Etil, butil, heksil, atau oktil). Sifat substituen ini secara langsung mempengaruhi sifat -sifat fizikal cecair ionik yang dihasilkan, seperti kelikatan, kestabilan haba, dan titik lebur. Rantai alkil yang lebih pendek biasanya menghasilkan interaksi ionik yang lebih kuat dan peningkatan kristal, yang membawa kepada titik lebur yang lebih tinggi. Sebaliknya, rantai yang lebih panjang meningkatkan hidrofobisiti dan dapat menindas kristal, berpotensi menurunkan titik lebur.
Di sisi anionik, PILS menggabungkan pelbagai kaunter, termasuk:
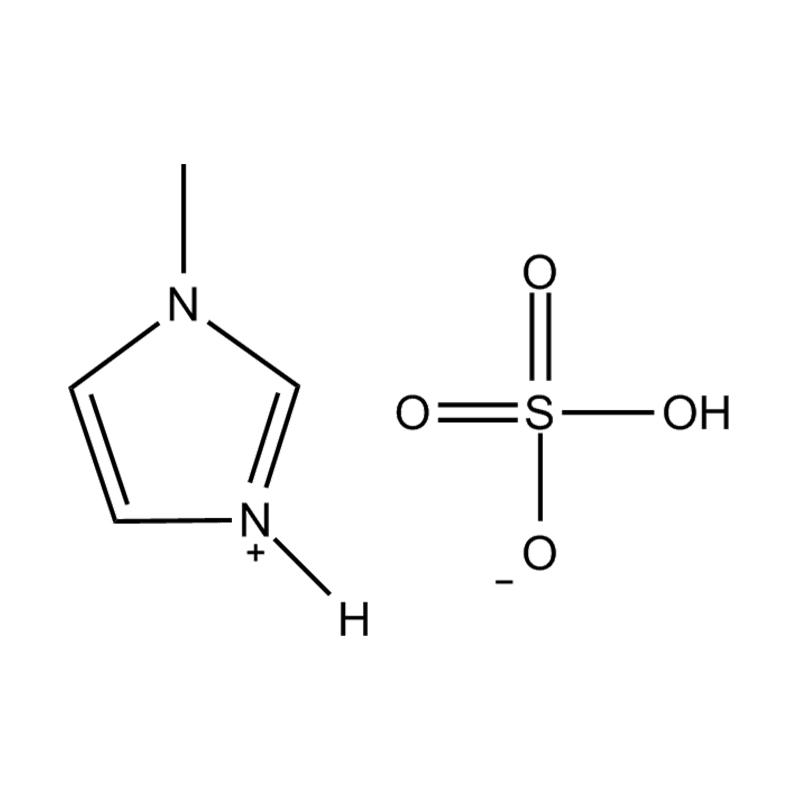
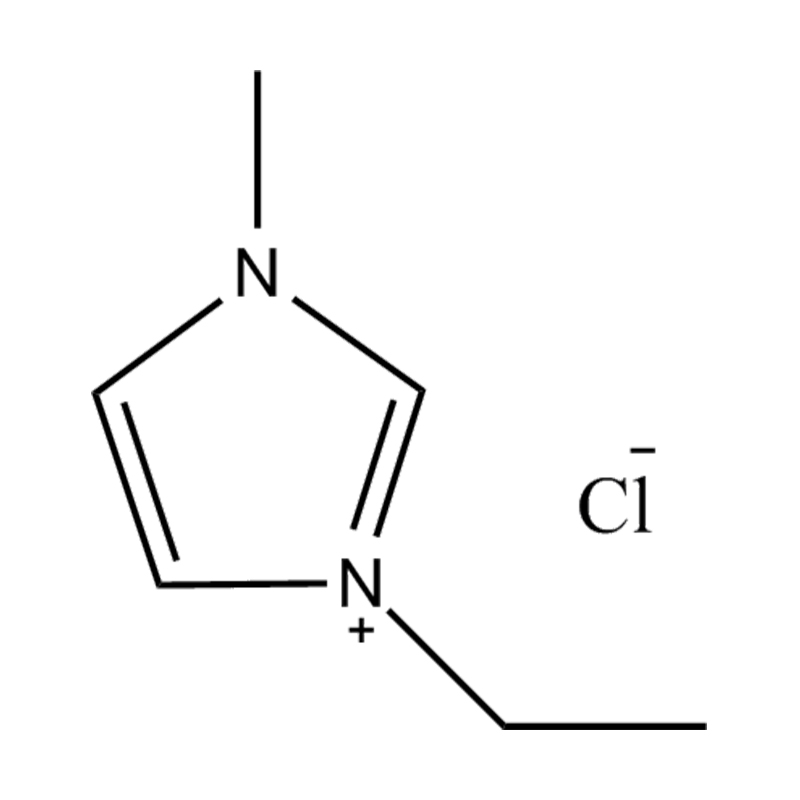
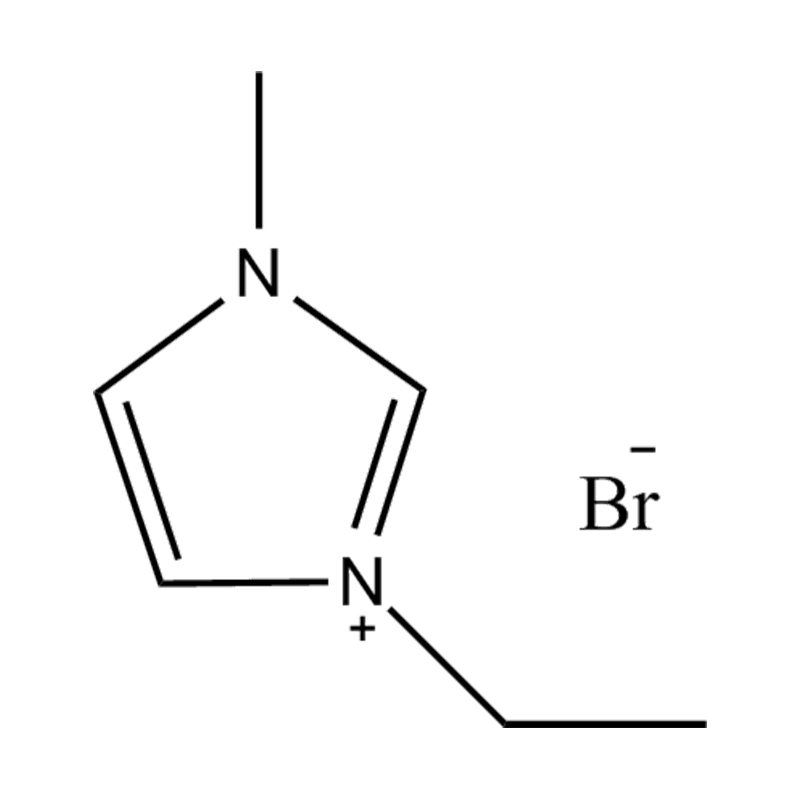
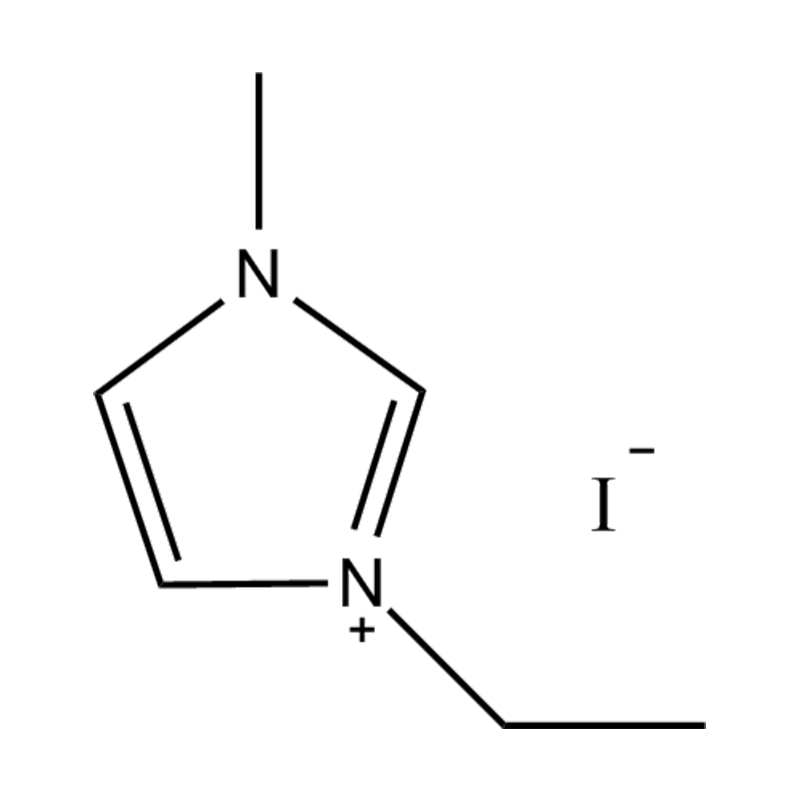
Halida: klorida (CL⁻), bromida (Br⁻)
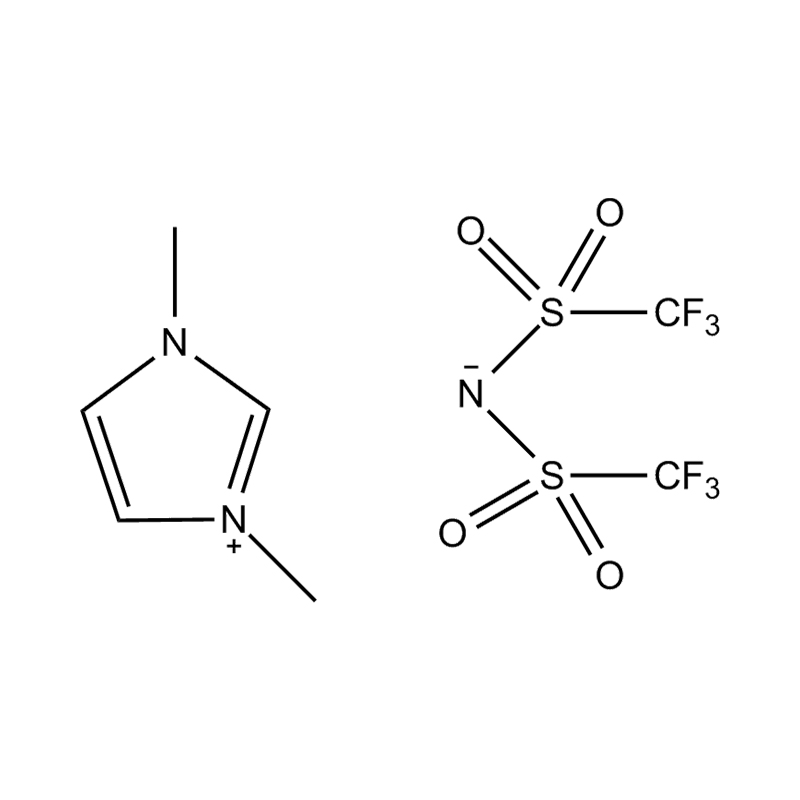
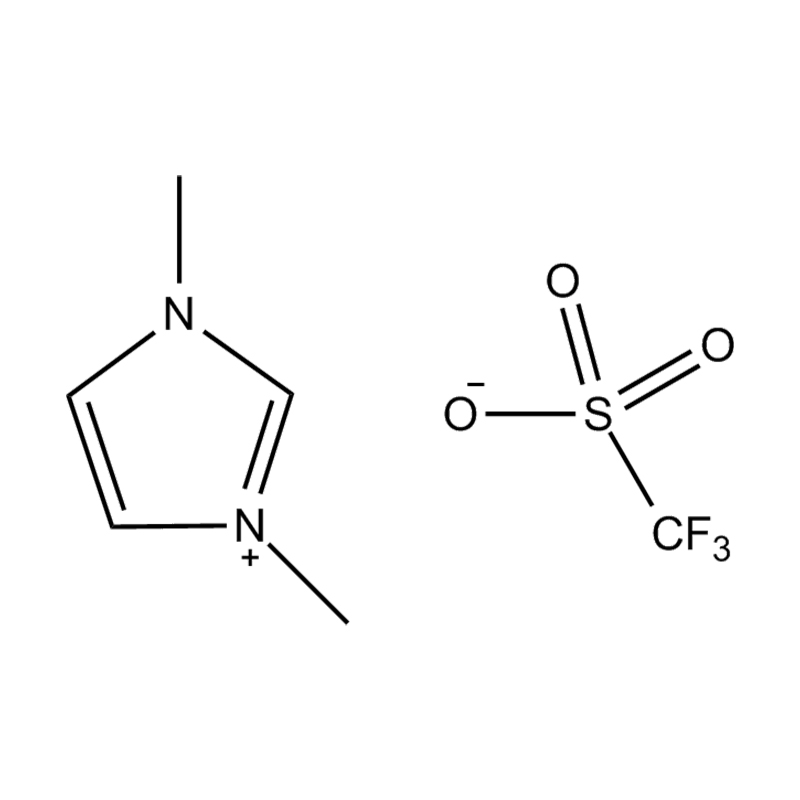
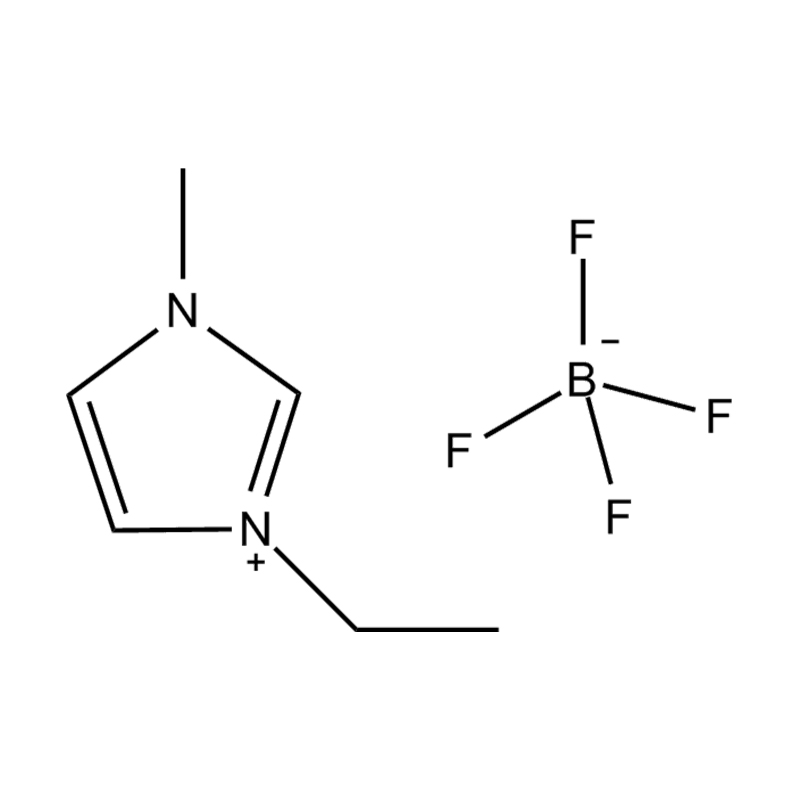
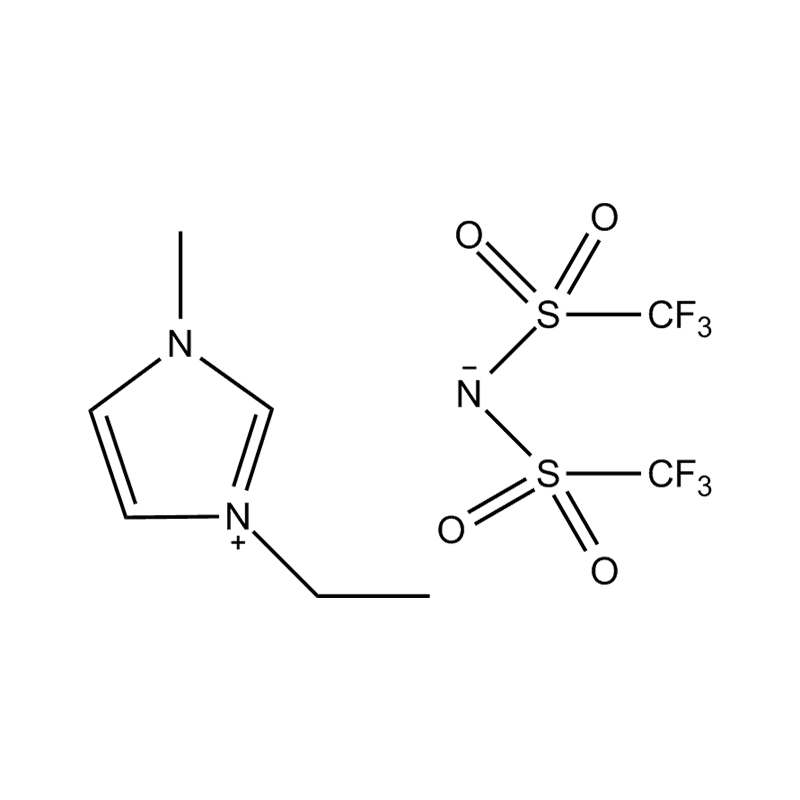
Anion fluorinated: tetrafluoroborate (bf₄⁻), hexafluorophosphate (pf₆⁻), bis (trifluoromethanesulfonyl) imide (ntf₂⁻)
Setiap anion memberikan ciri -ciri termal, kimia, dan pelarut tertentu. Sebagai contoh, NTF₂⁻ dikenali untuk menyampaikan kelikatan yang rendah dan kestabilan terma yang tinggi, menjadikannya sangat menarik untuk sistem suhu tinggi dan hidrofobik.
Sifat fizikokimia
Ciri -ciri fizikokimia PILs berkait rapat dengan interaksi antara kation dan anion. Titik lebur, selalunya lebih tinggi daripada cecair ionik biasa yang lain seperti derivatif imidazolium atau pyrrolidinium, adalah faktor pembatas kritikal. Ini sebahagian besarnya dikaitkan dengan sifat aromatik planar cincin pyridinium, yang menggalakkan pengumpulan π-π yang kuat dan memerintahkan pembungkusan dalam keadaan pepejal.
Walaupun demikian, cecair ionik pyridine mempamerkan ciri -ciri yang menggalakkan dalam beberapa aspek:
Kestabilan terma: Banyak PIL terurai pada suhu melebihi 200 ° C, menjadikannya sesuai untuk aplikasi suhu tinggi.
Tingkap Elektrokimia: Mereka sering menunjukkan tetingkap elektrokimia yang luas, penting untuk aplikasi elektrokimia.
Keupayaan solvation: Bergantung pada anion, PILs dapat membubarkan pelbagai bahan organik, bukan organik, dan polimer.
Hubungan struktur -struktur
Memahami hubungan struktur -harta dalam PILS adalah penting untuk menyesuaikan tingkah laku mereka kepada tugas -tugas tertentu. Hubungan utama termasuk:
Panjang rantai alkil vs kelikatan dan titik lebur: Meningkatkan panjang rantai alkil umumnya mengurangkan titik lebur tetapi meningkatkan kelikatan.
Jenis anion vs hydrophobicity dan kestabilan: anion fluorinated seperti PF₆⁻ dan NTF₂⁻ meningkatkan kestabilan haba dan elektrokimia, sementara halida memberikan kekonduksian yang lebih tinggi tetapi kekukuhan haba yang lebih rendah.
Kation planarity vs pembungkusan keadaan pepejal: Sifat planar cincin pyridinium menyumbang kepada titik lebur yang lebih tinggi disebabkan oleh pembentukan kekisi ionik yang lebih kuat.
Skop permohonan
Walaupun tidak digunakan secara meluas sebagai cecair ionik lain, cecair ionik piridin telah menunjukkan potensi dalam beberapa bidang niche dan baru muncul:
Sistem Elektrokimia
Oleh kerana kekonduksian ionik dan kestabilan elektrokimia, PIL adalah calon untuk elektrolit dalam bateri, kapasitor, dan sel bahan bakar. Penyelarasan kedua -dua struktur kation dan anion membolehkan pengoptimuman dalam voltan dan kekonduksian tertentu rejim.
Pemangkinan dan media reaksi
PIL telah disiasat sebagai pelarut dan pemangkin bersama dalam tindak balas organik, terutamanya dalam transformasi yang mendapat manfaat daripada media ionik dengan volatiliti yang rendah dan ketahanan haba yang baik.
Teknologi pengekstrakan dan pemisahan
Kelarutan selektif PIL membolehkan penggunaannya dalam sistem pengekstrakan cecair cecair untuk ion logam, bahan pencemar organik, dan biomolekul.
Pemprosesan bahan dan pempolimeran
Sesetengah kajian meneroka PIL sebagai pelarut atau aditif dalam tindak balas pempolimeran, yang mendapat manfaat daripada polariti dan sifat terma mereka.
Cabaran dan pandangan
Cabaran utama yang membatasi penggunaan PIL yang lebih luas kekal sebagai titik lebur yang agak tinggi, terutama bagi mereka yang mempunyai rantai alkil pendek dan anion halida mudah. Strategi untuk menangani ini termasuk penggunaan kumpulan alkil asimetrik, penggabungan anion besar atau fleksibel, dan sintesis campuran berasaskan PIL atau sistem eutektik.
Perkembangan masa depan juga boleh memberi tumpuan kepada fungsi cincin pyridinium dengan kumpulan reaktif atau penyelarasan tambahan untuk membolehkan interaksi khusus dalam pengiktirafan, penginderaan, atau pengiktirafan molekul. Dengan peningkatan permintaan untuk pelarut yang pelbagai dan struktur yang pelbagai, minat yang diperbaharui dalam cecair ionik piridin dijangkakan.
Cecair ionik pyridine menawarkan kelas sebatian yang kaya dan berfungsi secara fungsian dalam keluarga cecair ionik yang lebih luas. Walaupun penggunaannya kini dikekang oleh sifat terma, penyelidikan berterusan dalam pengoptimuman struktur -struktur boleh membuka kunci pelbagai aplikasi yang lebih luas. Ciri -ciri elektrokimia yang unik, tingkah laku solvation, dan reka bentuk modular menjadikan mereka calon yang menjanjikan untuk aplikasi khusus dalam elektrokimia, pemangkinan, dan pemprosesan bahan.



 中文简体
中文简体